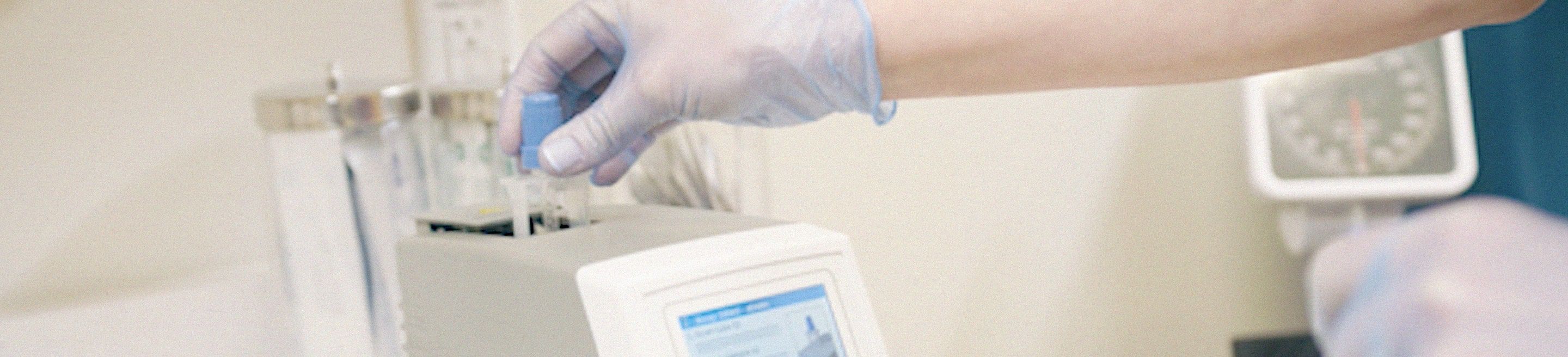
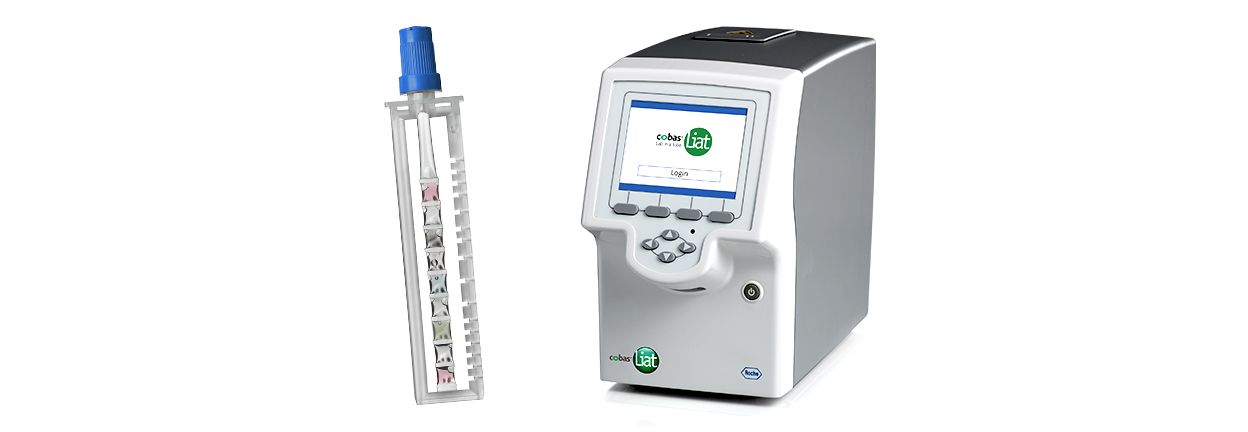
的cobas®用于SARS-CoV-2和流感A/B核酸检测cobas®Liat®系统 (cobas®SARS-CoV-2 & Influenza A/B)是一种用于同时快速的自动多重实时RT-PCR检测方法体外卫生保健提供者采集的鼻咽拭子中SARS-CoV-2、流感A、流感B病毒RNA的定性检测与鉴别,以及自己从疑似呼吸道病毒感染个体收集的鼻拭子(在卫生保健提供者的指导下在卫生保健环境中收集),与COVID-19一致,由卫生保健提供者收集。SARS-CoV-2与流感引起的呼吸道病毒感染的临床症状和体征可能相似。
cobas®SARS-CoV-2和流感A/B用于同时快速体外SARS-COV-2,流感病毒和流感B病毒核酸的检测和分化在临床标本中,并不旨在检测流感C病毒。在感染的急性期间,SARS-COV-2,流感A和流感B病毒RNA通常可在呼吸样本中检测到。阳性结果表明是主动感染,但不排除细菌感染或与其他未检测到的病原体合并感染。临床相关的病史和其他诊断信息是必要的,以确定患者感染状态。检测到的代理人可能不是疾病的确定原因。
阴性结果并不排除SARS-CoV-2、甲型流感和/或乙型流感感染,不应作为诊断、治疗或其他患者管理决策的唯一依据。阴性结果必须与临床观察、病史和/或流行病学信息相结合。
cobas®SARS-CoV-2和流感A/B供卫生专业人员或熟练使用cobas®Liat®系统。
在美国,测试用的是cobas®根据《1988年临床实验室改进修正案》(CLIA), 42 U.S.C.§263a认证的实验室有权进行中度或高度复杂的检测。cobas®SARS-COV-2和流感A / B也被授权用于护理(POC),即在豁免证书,合规证书或认证证书的患者护理环境中使用。在美国及其地区内的测试设施需要向适当的公共卫生当局报告所有SARS-COV-2结果。在美国。,cobas®SARS-CoV-2和流感A/B只适用于食品和药物管理局紧急使用授权。
在美国:
•该测试未获FDA批准或批准;
•该测试已通过FDA EUA授权,供授权实验室使用;
•本检测仅授权用于SARS-CoV-2、甲型流感病毒和乙型流感病毒核酸的同时定性检测和鉴别;对任何其他病毒或病原体均不适用;和
•这一测试仅在声明有正当理由授权紧急使用的情况存在期间被授权进行体外根据该法第564(b)(1)条,21 U.S.C.§360bbb- 3(b)(1)条,用于检测和/或诊断COVID-19的诊断测试,除非授权提前终止或撤销