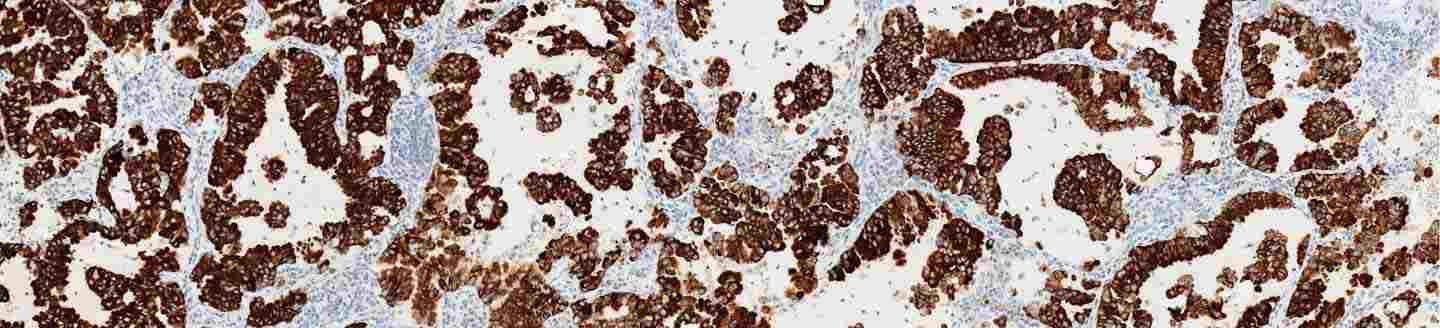
- 到2021年,美国将有约23.5万人被诊断出肺癌,其中非小细胞肺癌(NSCLC)占所有肺癌的84%1
- ALK -间变淋巴瘤激酶-是在NSCLC中发现的重要生物标志物,与之前的标准治疗相比,靶向治疗已被证明能显著提高无进展生存期2、3、4
- VENTANA ALK (D5F3) CDx Assay5现已被FDA批准作为四种靶向治疗的伴随诊断,为肺癌患者提供了更多的选择
2021年3月9日,图森-罗氏(SIX: RO, ROG;OTCQX:RHHBY今天宣布,美国食品和药物管理局(FDA)批准VENTANA ALK (D5F3) CDx Assay作为伴发诊断,以识别符合辉瑞药物lorlatinib治疗条件的ALK阳性非小细胞肺癌(NSCLC)患者。VENTANA ALK (D5F3) CDx检测是FDA批准的唯一一种作为LORBRENA伴发诊断的免疫组化(IHC)检测。
在之前的研究中,ALK阳性患者接受ALK抑制剂治疗后,无进展生存期可达近3年。2相比之下,ALK抑制剂研究中ALK阳性患者接受化疗的无进展生存期为7至8个月。3,4
FDA的批准对alk阳性患者来说是个好消息,
罗氏病理客户部门负责人吉尔·German说。
我们必须快速准确地识别出具有这种癌症生物标志物的患者,以便对他们进行有效的靶向治疗。这一标签扩展推进了罗氏对个性化医疗的承诺,为肺癌患者提供了更多的治疗选择,与标准护理相比,有更好的无进展生存机会。
VENTANA ALK (D5F3) CDx Assay现已被FDA批准作为四种靶向治疗的辅助诊断- XALKORI®(crizotinib), ZYKADIA®(ceritinib), ALECENSA®(alectinib)和LORBRENA®(lorlatinib)。研究表明,与原位荧光杂交(FISH)检测相比,该检测可识别更多可能受益于抗alk靶向治疗的NSCLC患者。6、7、8、9VENTANA ALK (D5F3) CDx Assay在美国可用于BenchMark ULTRA和BenchMark XT免疫组织化学/原位杂交(IHC/ISH)载片染色仪器。